第1章 太陽系の概要と地球大気
1.太陽の概観
太陽は巨大なガス球であり、主成分は水素77.3%,ヘリウム21.4%,酸素0.84%などで構成されています。太陽の半径は約7×10
5kmで、地球の半径(6.4×10
3)の約100倍であり体積は100万倍です。中心部の水素の核融合反応によってエネルギーはつくられており、光球とよばれる太陽の表面温度は約6,000Kです。太陽から地球へ届くエネルギーは電磁波の一種であり、波長の短い順に紫外線,可視光線,赤外線などとなっています。太陽放射エネルギーの大部分は0.2~4μmの波長領域であり、全放射エネルギーの約半分は可視光領域(0.38~0.77μm)にあります。太陽放射は、地球の大気を素通りして地表面で吸収されて地球を暖め、低気圧や台風などの発生、雨や風、雲など地球上で起こる気象現象の原因となっています。
図1 太陽のようす
2.惑星の大気
太陽系の惑星は
地球型惑星と
木星型惑星に2種類があります。地球型惑星は水星,金星,地球,火星であり、硬い地殻(岩石表面)で構成されている小さな惑星です。木星型惑星は木星,土星,天王星,海王星であり、基地で構成されている巨大な惑星です。
図2 太陽系の惑星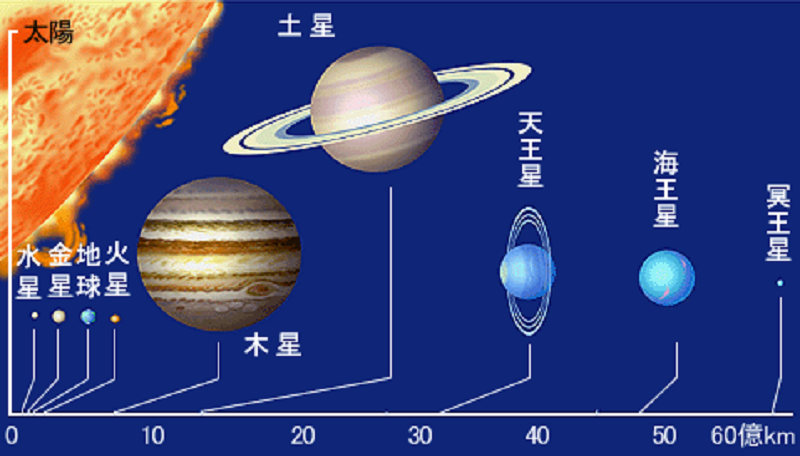
(1)地球型惑星
水星:
重力が小さく太陽風が強いために大気は飛ばれていてほとんどありません。太陽に近いため高温であり表面温度は560K(⇒約300℃)です。
金星:
大気は厚く濃いです。気圧は地球の90倍です。大気組成は二酸化炭素が主で約96%以上で、表面温度は720K(⇒約450℃)です。以前は地球と大きさも密度も似た双生児と思われていました。
地球:
大気組成は窒素と酸素が主で二酸化炭素は少量でで、表面温度は288K(⇒15℃)。
火星:
大気は薄く地球の7%程度です。大気組成は二酸化炭素が主で約95%以上で、表面温度は180K(⇒約-100℃)です。二酸化炭素は凍結してドライアイスの状態です。
(2)木星型惑星
木星や土星の大気の主成分は太陽と同じ水素とヘリウムで構成されています。天王星と海王星の大気の主成分は水素とヘリウムです。
表1 太陽系の惑星の特性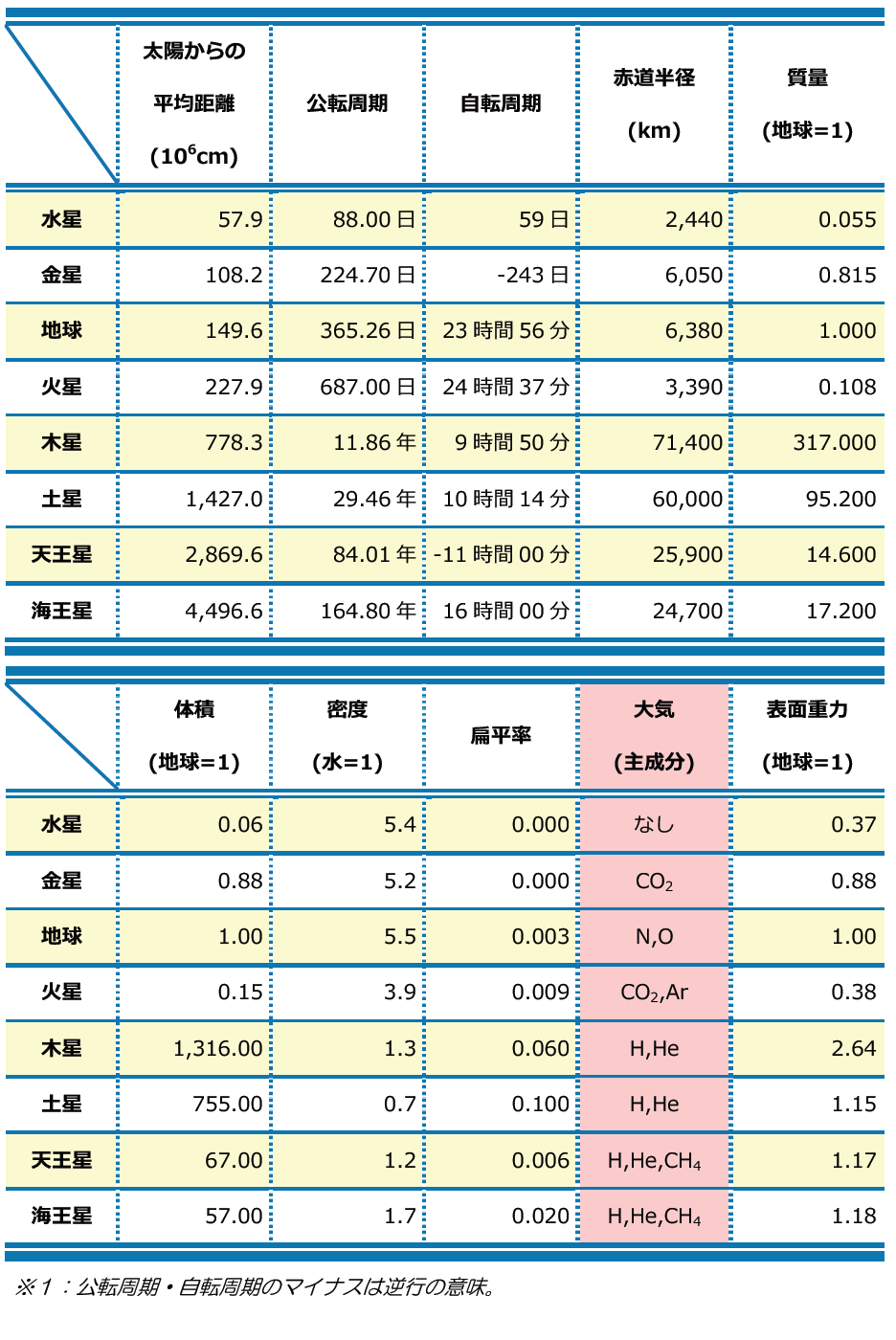 表2 地球型惑星の特性比較
表2 地球型惑星の特性比較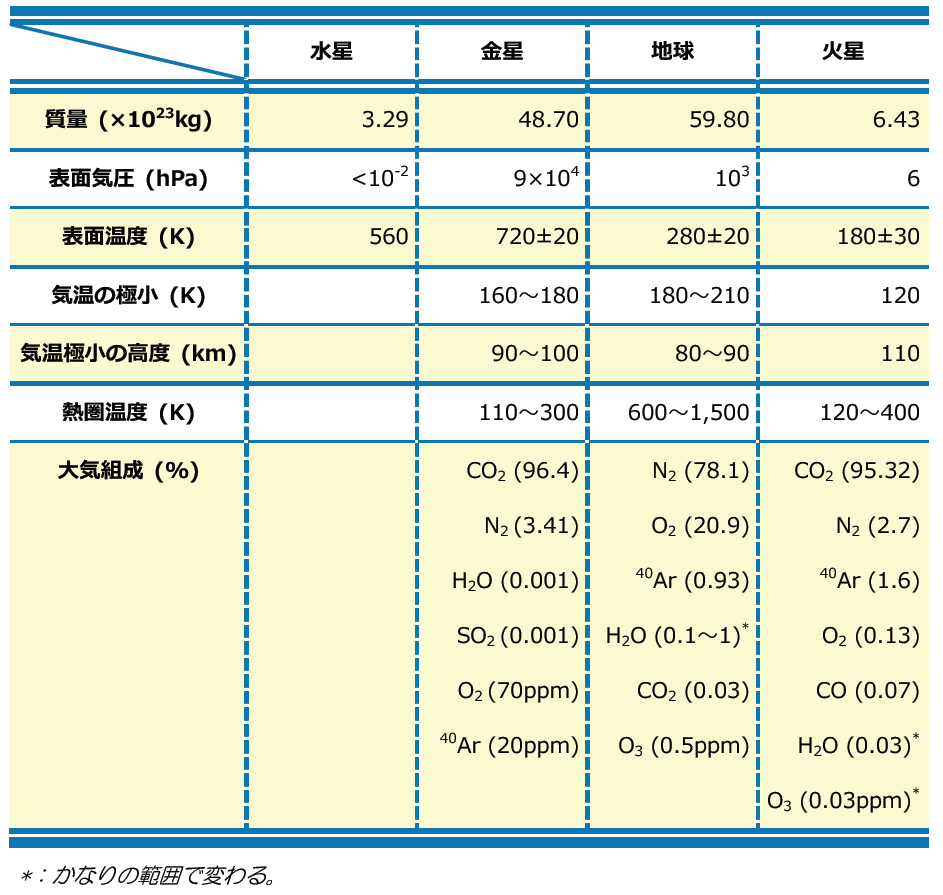
3.地球大気の特徴
(1)地球大気の組成
地球大気の組成は、窒素78%,酸素21%,アルゴン0.93%,二酸化炭素0.03%と他の惑星と大きく異なっています。この組成は高度8万m(⇒中間圏圏界面)までほぼ一定です。
表3 地表付近の大気組成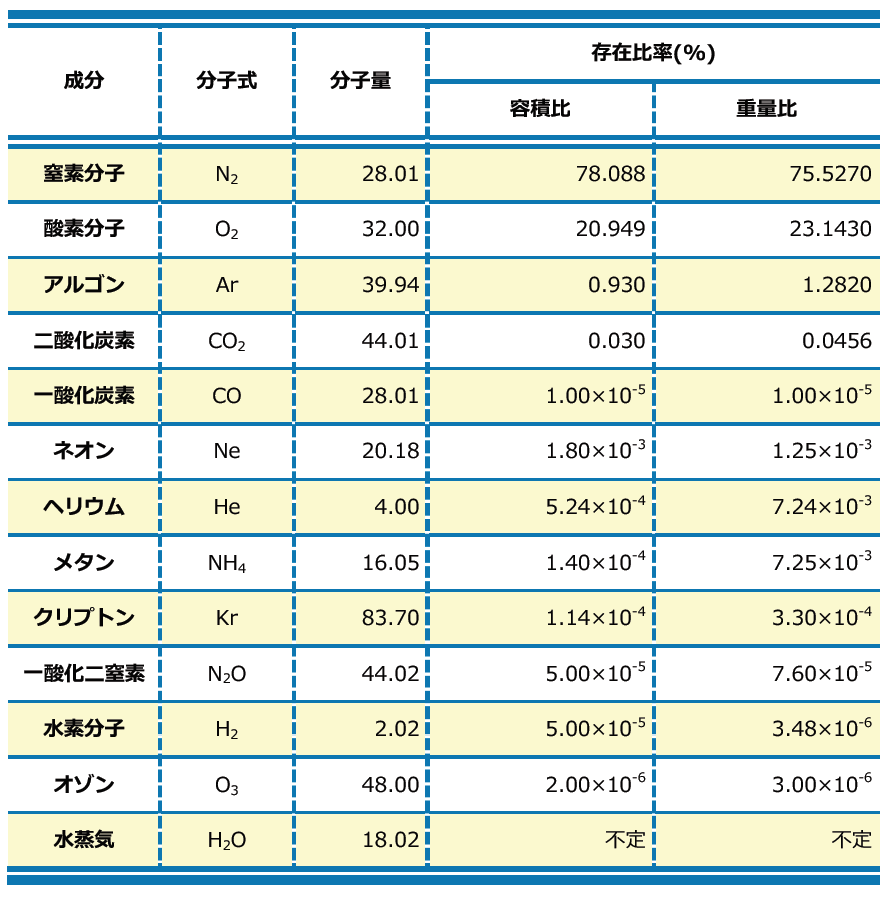 図3 大気圧の鉛直変化
図3 大気圧の鉛直変化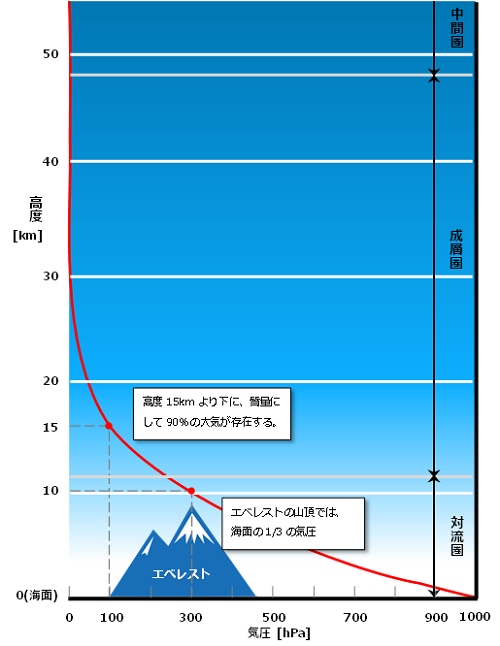
(2)初期の大気
地球の大気は、火山噴火などで地球内部から出てきたガスによって生成されました。原始の地球大気は、太陽と同じ水素とヘリウムを主成分と考えられていますが、太陽風で吹き払われてしまいました。その後、火山の噴火などにより地球内部から水蒸気88%,二酸化炭素6%,窒素2%,硫黄と鉄1~2%,塩素0.3%,アルゴン0.1%以下などが噴出し、現在の地球大気の材料がそろいました。
(3)水蒸気と海の起源
現在の地球表面にある水は14億km
3といわれています。そのうちの97%は海水で、次に南極大陸や北極大陸にある氷が2.4%、淡水(地下水)が0.6%、淡水(湖沼,河川など)が0.02%であり、地球大気中の水蒸気はほんのわずかな0.001%といわれています。大気中に含まれる水蒸気が少ないのは、大気が含み得る水蒸気の量には限度があるからです。このため、地球内部から噴出ガスとして大量の水蒸気が大気中に放出されて、それが雲となり膨大な量の雨や雪を降らせました。その雨や雪が冷えつつあった地球表面の低い地域に集まって海ができました。この海がいつできたのかは確定できていませんが、約38億年前の古い堆積岩を源岩とする変成岩が存在することからその頃ではないかといわれています。初期の海洋は火山ガスである硫黄や塩素の化合物が溶け込んだ強い酸性であり、噴出した二酸化炭素や窒素は酸性の海に溶け込めず大気に残ったので、この頃の地球大気は金星や火星と同様の二酸化炭素や窒素であったと考えられています。酸性の強い海に、やがて岩石を構成している鉱物から溶け出した鉄やアルミニウム、カルシウム、マグネシウムなどの金属イオン(⇒水に溶けるとアルカリ性を示す)によって中和されました。中和した海に大気中の二酸化炭素が大量に溶け込み、大気には窒素が残りました。
表4 地球表面上の水分の存在形態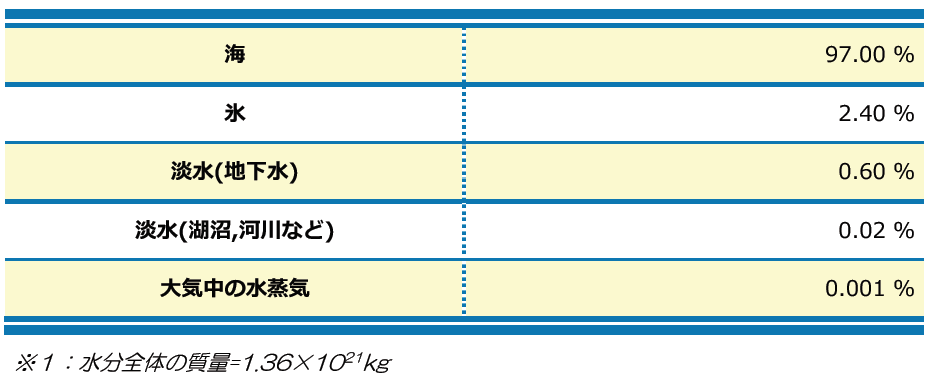 表5 地球表層における炭素の分布形態
表5 地球表層における炭素の分布形態
(4)酸素の生成
地球の大気に多くある酸素は植物の光合成によって生成されました。原始の地球大気は現在の大気と違って、太陽光線の中の紫外線が減衰することなく地表面に達していたために、生物は住めない状態でした。しかし、海中深いところまでは紫外線が届かなかったために海の中で酸素を必要としないバクテリアが誕生しました(⇒地球最初の生命体の誕生は約35億年前です)。さらに光合成をする植物(藍藻類)が生まれ、進化した緑藻類が二酸化炭素を吸収して酸素を発生させるようになり、大気中に酸素が増加し始めました。その後、酸素と紫外線の光化学反応によって、大気中にオゾン層が形成されると、生物に有害な紫外線がオゾン層によって吸収され、地表に達する紫外線の量が少なくなりました。これにより生物は海から出て地上でも生活できるようになりました。
4.地球大気の鉛直構造
地球をおおっている大気の範囲を
大気圏といいます。大気圏は上空に行くにしたがって次第に希薄になっていきます。その上限は80万~100万mです。大気の温度(⇒気温)や圧力(⇒気圧)は場所によっても変わりますが、高度によって大きく変化します。変化の大きい大気なので、航空機の運航などのためにきじゅんとなる大気の平均状態を示した国際標準大気を設定しています。大気圏は下層から、
対流圏,
成層圏,
中間圏,
熱圏となっています。対流圏と成層圏はの境界面は
対流圏界面、成層圏と中間圏の境界面は
成層圏界面、中間圏と熱圏の境界面は
中間圏界面と呼ばれています。
図4 対流圏の高さ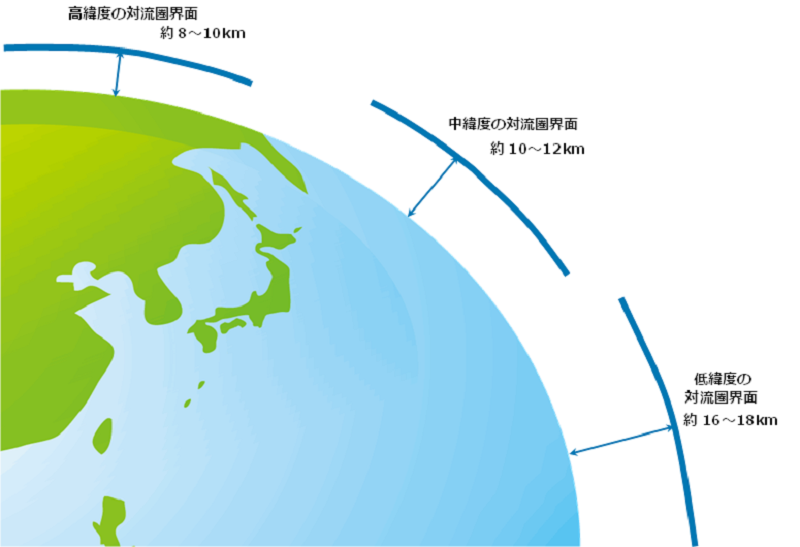 図5 気温とオゾン量の鉛直分布と大気層の区分
図5 気温とオゾン量の鉛直分布と大気層の区分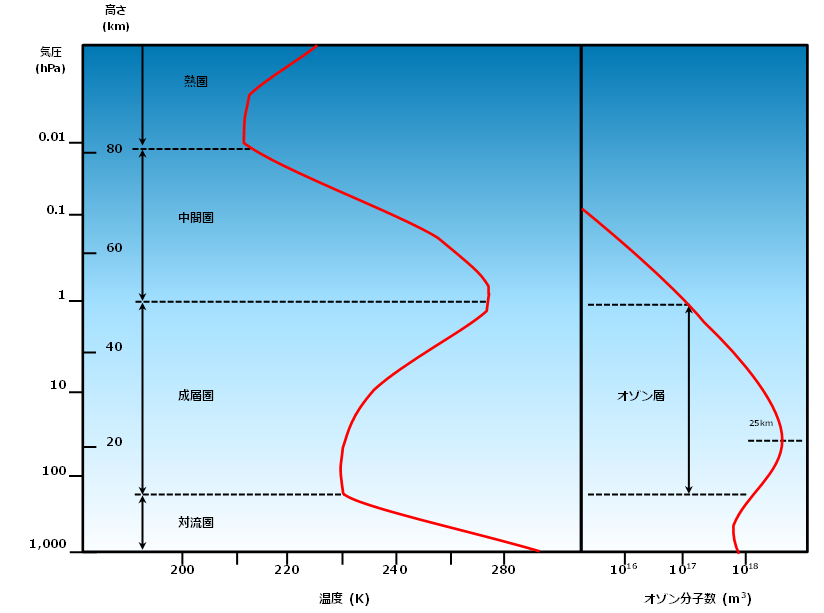
(1)対流圏
対流圏は地表~平均約11,000mまでの範囲をいいます。対流圏界面は、赤道付近の低緯度では約16,000m、北極や南極などの高緯度では約8,000mです。中緯度では平均的には約11,000mですが、季節変化や低気圧や高気圧の動向によって高くなったり低くなったり変化しています(⇒夏は高く、冬は低い)。対流圏での気温減率は、平均的には約6.5℃/kmです。上空にいくほど気温が低くなっていますが、それは太陽光線のほとんどは大気を通過して地表を暖め、大気は地表からの熱で暖まるために下層ほど暖かく上空にいくほど低くなっています。台風や低気圧、高気圧、雨や雪などの気象現象のほとんどは、この対流圏の中で発生しています。
(2)成層圏
成層圏は約11,000m~約50,000mまでの範囲をいいます。高度約20,000mまでは気温は一定(約220K(⇒約-50℃))ですが、それより上空では高度とともに気温が上昇して約50,000m付近の成層圏界面では約270K(⇒約-3℃)と極大になります。対流圏と違って空気は上下に混ざりにくく安定した層なので成層圏と名づけられました。成層圏の20,000~30,000m(極大は25,000m付近)にオゾン層が存在します。高度20,000m付近から気温が上昇するのは、オゾンが太陽からの紫外線を吸収し熱エネルギーに変えて空気を暖めているからです。
(3)中間圏
中間圏は約50,000~約80,000mまでの範囲をいいます。高度とともに気温は低下します。気温減率は対流圏の半分以下です。中間圏界面(⇒約80,000m)のところで気温が約180K(約-90℃)と極小で、大気圏中で最低になっています。これは中間圏には熱源がないため、赤外放射による温度低下のためです。地表から中間圏の80,000mまでは、水蒸気を除いた大気の化学組成の割合は高度によらず一定ですが、ここから上層では重力による分離がはじまり、大気組成は軽い気体(ヘリウム,水素)の分子や原子の割合が多くなります。
(4)熱圏
熱圏は約80,000~約500,000mまでの範囲をいいます。高度とともに気温は上昇し、500,000mでは約1,000K(⇒約700℃)となっています。この高温の原因は、太陽からの紫外線が熱圏にある窒素や酸素に吸収されるためです。熱圏では、短い波長の紫外線やX線での吸収により空気の成分である窒素や酸素の分子や原子が光電離されています。この電離された密度の大きい層を
電離層(⇒高度約100,000~300,000m)といいます。電離層の中でも特に電子の多い層が3つあり、下から
E層,
F1層,
F2層と呼ばれており、さらにE層の下に
D層と呼ばれる弱い電離層があります。電離層は、地上から発射された電波を反射する性質があり、通信などに利用されています。熱圏の気温は太陽紫外線の強さによって決まっていて、1日に数100℃も変化することがあるほか、太陽活動の影響を受けて500~2000K(⇒200~1700℃)にも変化します。
図6 電離層のE,F1,F2層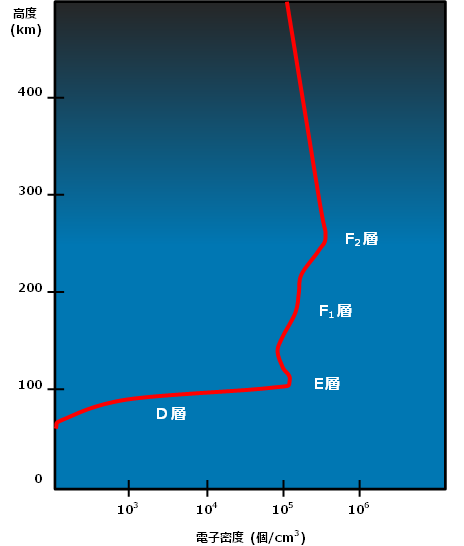 図7 熱圏内の温度の高度分布
図7 熱圏内の温度の高度分布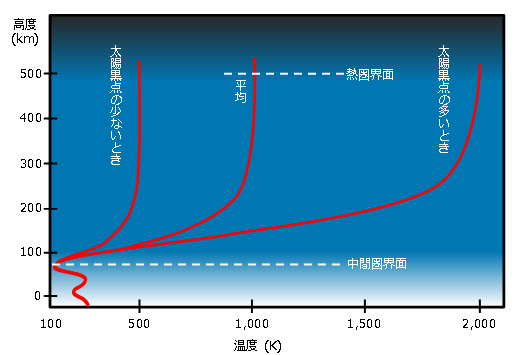
(5)外気圏
熱圏との境界である500,000m以上の空間で、この上は宇宙空間です。
5.オゾン層とオゾンホール
成層圏では、太陽からの紫外線を吸収してオゾン層がつくられます。オゾン密度が極大になるのは、成層圏下層の高度約25,000m付近です。オゾン量が多いといっても、その数は大気分子約100万個に対してわずか1個程度の量です。全地球大気の中に占めるオゾン総量の割合は、1/100万に過ぎないです。
(1)オゾン層の役割
微量のオゾン量だが、太陽からの有害な紫外線を吸収し、人間をはじめ地球上の生物の生命を守ってくれる防御層(バリア)になっています。
(2)オゾン生成のしくみ
A.大気中の酸素分子(O2)が太陽紫外線(0.24μm以下の波長領域)を吸収することによって、2つの酸素原子(O)に分解されます。
O2 + 光(紫外線0.24μm以下)---> 2O
B.分解された酸素原子がそれぞれ別の酸素分子と結合してオゾン(O3)が生成されます。
O2 + O ---> O3
C.一方、生成されたオゾンは、太陽紫外線(0.25~0.32μmの波長領域)を吸収することによって、オゾン分子が酸素原子に分解されて消滅します(B.の逆の化学反応)。
成層圏ではこうしたオゾンの生成と消滅を繰り返すことによってオゾン層が一定に保たれています。
図8 オゾン生成のしくみ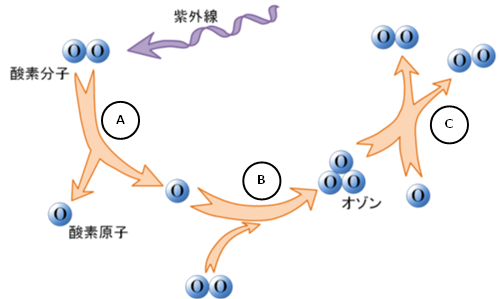
(3)オゾンの分布
オゾンは、主に低緯度(赤道付近)の成層圏でつくられ、大気の流れによって成層圏全体に広がっていきます。しかし、その量の緯度分布は、平均的にみて低緯度(赤道方面)で少なく、高緯度(極方面)を中心に多くなっています。紫外線の多い低緯度で極大になりそうですが、実際には高緯度に多いのは、成層圏下層では地球規模の大気大循環(⇒熱の高緯度への輸送)などによって低緯度から高緯度への流れがあり、低緯度の成層圏で生成されたオゾンが冬に高緯度へと運ばれるためです。これを、
ブリューワー・ドブソン循環といいます。季節変化は、北半球では3~4月の春に、南半球では10月の春に、それぞれ北極・南極に近い高緯度で極大となっています。
表6 緯度別・月別のオゾン分布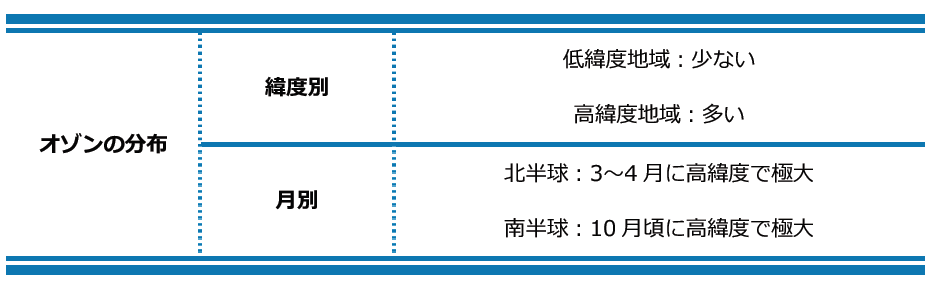 図9 成層圏と対流圏における大気の流れによるオゾンの輸送
図9 成層圏と対流圏における大気の流れによるオゾンの輸送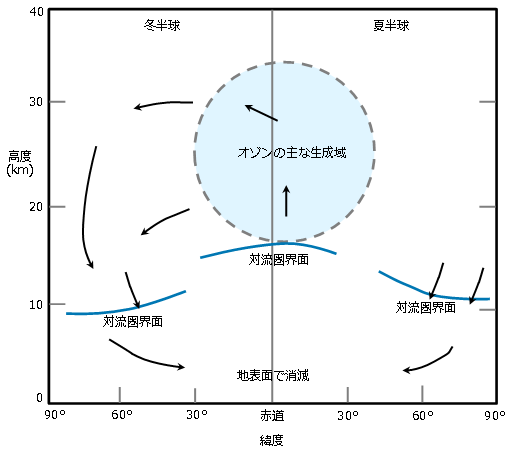
(4)オゾン層の破壊とオゾンホール
オゾン層の破壊の原因は、フロンが分解して放出された塩素であり、塩素分子がオゾンを酸素原子に分解して極地域のオゾンを減少させます。オゾン層の破壊による影響は、地球上に有害な紫外線が降り注ぐことにより、白内障や皮膚ガンの増加、植物の成長や農作物の収穫の低下、動植物の生態系や気候の変化などがある。オゾン層の破壊は、1970年代後半から1980年代の南極にて春にオゾンの少ない領域が現れ、その範囲が毎年拡大していくことから判明しました。オゾンホールの発見は1982年に日本の南極観測隊が発見しました。オゾン層の破壊の原因となるフロンは、人体には無害なために冷蔵庫やエアコンの冷媒、スプレーの噴出剤、半導体の洗浄などに広く使われてきた自然界には存在しない人工的に作り出された化学物質です。化学的に非常に安定した気体であるため、大気中に放出されるとほとんど壊れないまま成層圏に達し、成層圏で紫外線によって分解して放出された塩素がオゾン層を破壊します。
(5)オゾン層の破壊のメカニズム
A.成層圏の上層に達したフロンは、太陽からの強い紫外線によって分解されて塩素原子(Cl)を放出します。
B.塩素原子は、オゾン分子(O3)と反応して酸素原子(O)1個を奪って一酸化塩素(ClO)になります。オゾン分子は消滅し、酸素分子(O2)になります。
Cl + O3 ---> ClO + O2
C.さらに一酸化塩素はすぐに酸素原子と反応して酸素分子となり、塩素原子を放出します。
ClO + O ---> Cl + O2
D.こうして塩素原子はオゾンが酸素分子に分解する際に有効な触媒として働き、それを繰り返しながらオゾン層を破壊していきます。
図10 オゾン層破壊のしくみ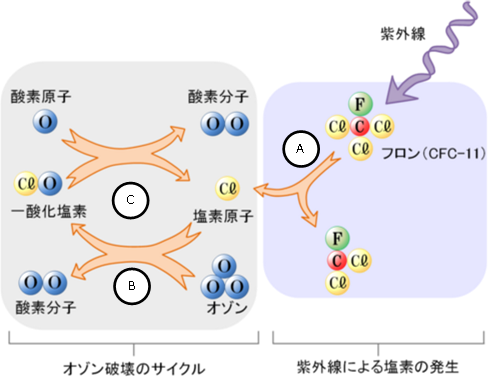
(6)オゾンホールのできる仕組み
南極の冬は太陽の光が射さないため(⇒極夜)、気温が非常に低くなります。成層圏の気温が氷点下78℃以下になると、凍った微粒子からなる極成層圏雲ができます。この極成層圏雲ができると、その雲粒表面での特殊な化学反応で大気中に大量の塩素分子が放出されます。この塩素分子はそのままではオゾン層を破壊することはありませんが、南極が春(10月)になって太陽の紫外線が成層圏に届くようになると、塩素分子と紫外線が反応して塩素原子がつくられ、これがオゾンを破壊してオゾンホールができるのです。












